
蛍光分光光度計・蛍光寿命測定装置
3次元蛍光(EEM)データの補正プロセスとAqualogソフトウェア
PARAFACモデルを用いた3次元蛍光分析における課題は,高精度なスペクトルが再現性良く得られるかということにある。このため以下のようなスペクトル補正を行うことが必須となる。(Figure 3)
- 励起波長の変化に伴う励起光出力の変化を打ち消すために,3次元蛍光データは各波長における蛍光と励起光の強度比によりあらわす。
- 装置間の比較を可能するために,モノクロメータや光路特性等,装置に特有なパラメータを補正する。
- DOMによる励起光の吸収と蛍光の再吸収 IFEs:Inner filter effects(インナーフィルター効果)を補正する。
Figure 3 Flow chart for instrumental, spectral and Inner-Filter Effect correction for EEMs of CDOM
超純水のEEMマップ
Figure 4Aは超純水(ブランクとして)のEEMマップを示す。ここには励起光の1次光および2次光のレイリー散乱によるラインが読み取れる。これは分光器のグレーティング反応によるものである。またFigure 4Aには水のラマン光散乱によるラインも読み取れる。水のラマン光散乱はレイリー散乱に対して常に3,328㎝-1エネルギーシフトした波長に現れる。CDOM成分のライブラリーは人為的なレイリー散乱や水のラマン光散乱のスペクトルは取り除かれたスペクトルとなっている。このためEEMデータはこのような不要な散乱光ピークを取り除いておく必要がある。
Figure 4BはCDOMサンプルから得られた未補正のE E M生データを示す。これは国際腐植物学会(IHSS)より取り寄せたポニー湖(Pony Lake)のフルボ酸(PLFA)の標準試料の分画である。ここではCDOM成分と一緒にレイリー光散乱や水のラマン光散乱のラインも等高線マップ上に表示されている。Aqualogのソフトウェアを用いればこのようなレイリー散乱光を簡単に削除することができる。
Figure 4CはFigure 4Bの未補正のEEM生データからFigure 4Aのブランクを差し引いた結果を示している。
さらにFigure 4DはFigure 4Cのデータからさらに1次光,2次光のレイリー散乱を消し込んだアルゴリズムの結果を示す。硫酸キニーネ(QSU)の蛍光スペクトルデータを元にしてCDOMのEEMデータをノーマライズする[1,6,12]。AqualogのソフトウェアのEEMプロセシングを使えば水のラマン光と硫酸キニーネ(QSU)によるノーマライゼイションに簡単に対応することができる。レイリー散乱や水ラマン光散乱の補正に加えて,サンプルとブランクから同時に測定した紫外可視吸収スペクトルを使ってインナーフィルター効果によるEEM分析データの補正を行う。Aqualogのインナーフィルター効果のアルゴリズムを使って一次および二次のインナーフィルター効果を補正するためには励起スペクトルと蛍光スペクトルの両方がオーバーラップする領域の吸収スペクトルを測定することが必要となる。標準的な1㎝光路長のセルで測定する場合,CDOMによる蛍光の再吸収インナーフィルター効果(IFE)を以下の式により補正する[11]。

ここで,FidealはIFEがない理想的な(補正後の)蛍光強度,Fobsは測定した蛍光強度,AbsExとAbsEmは励起波長における試料の吸光度,AbsEmは蛍光波長における試料の吸光度を示す。装置間の比較を可能するために,分光器や検出器,光路特性等,装置に特有なパラメータを補正する。文献に書かれているアルゴリズムでは,光学上幾何学的なパラメータとしてセルの光路長,ビーム幅やスリット幅,励起光および蛍光ビーム光路に関連するセル配置や取換え等の装置固有のパラメータ等も説明される[10-13]。

- Figure 4? The fundamental instrument correction operations for processing an excitation emission map including blank subtraction and Rayleigh line nullification.
PLFAサンプルのEEMデータ
Figure 5Aと5Bは,254 nmのAbs=0.8の高濃度PLFAサンプルのEEMデータを示し,Figure 5Cと5Dは,254 nmのAbs=0.2の低濃度PLFAサンプルのEEMデータを示す。通常,光路長1 m,DOC濃度1 mg/Lあたりの254 nmにおける吸光度が用いられ,これはSUVA(もしくはSUVA254;Specific UV Absorption)と呼ばれる。254 nmでの吸光度はCDOM濃度を評価するための業界スタンダードとなっている[8,15]。
左側の上下のデータ(Figure 5Aと5C)は共に未補正のEEM生データ(Fobs)であり,右側の上下のデータ(Figure 5Bと5D)は共に補正済みのEEMデータ(Fideal)である。
Figure 5Aに示した未補正の高濃度PLFAサンプルのEEMデータでは励起波長(横軸)300 nm以上に(300 nm以下に比べて)顕著な発光ピークが表れている。このサンプルでは300 nm以下の紫外領域でインナーフィルター効果の影響が強いことがわかる。この波長領域では励起スペクトルと蛍光スペクトルがオーバーラップしている。高濃度PLFAサンプルのEEMデータにIFE補正を行ったものでは(Figure 5B),低濃度PLFAサンプルのEEMデータをほぼ同じようなパターンを示す。低濃度PLFAサンプルでは,Figure 5C(IFE未補正)とFigure 5D(IFE補正済)のデータを見比べてみるとわかるように,蛍光のパターンにほとんど差がないことがわかる。このようにCDOM濃度が高いサンプルについてはIFEの影響が大きいためIFEの補正を行うことが望ましい。
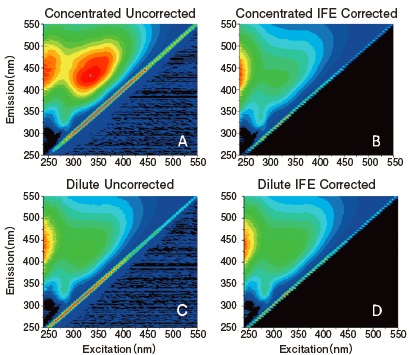
- Figure 5? A comparison of the influence of the inner-filter correction algorithm on excitationemission maps of concentrated?top row?and dilute?bottom row?samples of the Pony Lake Fulvic Acid standard sample.

- Figure 6? A comparison of the concentration dependence of the absorbance spectra?A and B? and the excitation spectra of the Pony Lake Fulvic Acid sample before?C and D?and afte?r E and F?inner-filter correction.
IFEの補正の重要性
Figure 6ではよりIFE補正の影響を詳しく示すために,可視紫外吸収スペクトルと,低濃度PLFAのEEMデータの励起スペクトルを比較している。
Figure 6Aは希釈の度合ごとのPLFAサンプルの紫外可視吸収スペクトルを示している。吸収スペクトルは特定のピークを示すことなく,紫外から可視領域において長波長になるに従い単調に減少している。
Figure 6BにはFigure 6Aに示した希釈の度合(横軸)と吸収スペクトルの254 nmでの吸光度(縦軸)のプロットを示す。
Figure 6BのデータからAbs=0.8付近の吸収のピークに至るまでサンプル濃度と吸光度には高い相関があることがわかる。
Figure 6Cでは励起スペクトルのFob(s 励起強度)をみると400 nmより短波長域で励起強度が大きく減っていることがわかる。
Figure 6Dでは,インナーフィルター効果が高まる,吸光度が0.2を超えるエリアでは,254 nmでの吸光度(縦軸)と励起強度(横軸)との間に相関が認められないことがわかる。
しかしながらFigure 6Eに示すように,インナーフィルター効果(IFE)の補正を行った励起スペクトルでは短波長域の強度が復活して,Figure 6Aの吸収スペクトルと同様なプロファイルが得られた。254 nmの励起強度(縦軸)と254 nmの吸収強度(横軸)にも高い相関が確認され,特に高濃度CDOMサンプルの分析におけるIFEの補正の重要性が確認できる。

